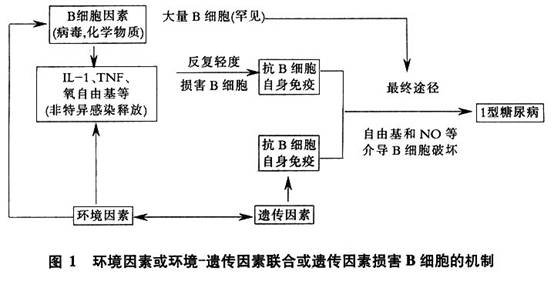
1型糖尿病确切的病因及发病机制尚不十分清楚,其病因乃遗传和环境因素的共同参与。主要由于免疫介导的胰岛B细胞的选择性破坏所致。 1.遗传因素 (1)家族史:1型糖尿病有一定的家族聚集性。有研究报告双亲有糖尿病史,其子女1型糖尿病发病率为4%~11%;兄弟姐妹间1型糖尿病的家族聚集的发病率为6%~11%;同卵双生子1型糖尿病发生的一致性不到50%。 (2)HLA与1型糖尿病:人类白细胞抗原(HLA)基因位于第6对染色体短臂上,为一组密切连锁的基因群,HLA由Ⅰ、Ⅱ、Ⅲ3类基因编码。Ⅰ类基因区域包括HLA-A、HLA-B、HLA-C和其他一些功能未明的基因及假基因,其编码的抗原分子存在于全部有核细胞的表面,负责递呈外来抗原给CD8的T淋巴细胞;Ⅱ类基因区域主要包括HLA-DR、HLA-DQ和HLA-DP3个亚区,分别编码DR、DQ和DP抗原,存在于成熟B淋巴细胞及抗原递呈细胞表面,负责递呈抗原给CD4细胞;Ⅲ类基因区域编码包括某些补体成分在内的一些可溶性蛋白,如C2C4A、C4B、肿瘤坏死因子(TNF)和热休克蛋白(HSP)等。HLA通过主要组织相溶性复合体(MHC)限制,参与T淋巴细胞识别抗原和其他免疫细胞的相互作用,以及自身耐受的形成和维持,在识别自身和异己、诱导和调节免疫反应等多个方面均具有重要作用。可见,HLA在许多自身免疫性疾病包括1型糖尿病的发生和发展中占有非常重要的地位。 现已证实某些HIA与1型糖尿病的发生有强烈的相关性。在一个有1型糖尿病的家族中,相同HLA抗原的兄弟姐妹发生糖尿病的机会为5%~10%,而非HLA相同的兄弟姐妹发生糖尿病的机会不到1%。在高加索人口中,95%1型糖尿病患者拥有HLA-DR3或HLA-DR4,而非糖尿病者为45%~50%;HLA-DR2对避免1型糖尿病的发生有保护作用。HLA-DQ基因是1型糖尿病易感性更具特异性的标志,决定B细胞对自身免疫破坏的易感性和抵抗性。有报告在伴有1型糖尿病HLA-DR3的病人中,几乎70%发现有HLA-DQw3.2,而保护基因HLA-DQw3.1则出现在DR4对照者。研究发现如果两个等位DQβ链的第57位被天门冬氨酸占位,一般将不易发生自身免疫性糖尿病,若两个等位点均为非天门冬氨酸则对1型糖尿病强烈易感,HLA-DQA1链第52位精氨酸也是1型糖尿病的易感基因。HLA-DQβ1链57位为非天门冬氨酸纯合子和HLA-DQA1链52位精氨酸纯合子的个体患1型糖尿病的相对危险性最高。DQβ链的45位氨基酸对抗原决定簇的免疫识别为DQw3.2而不是DQw3.1。上述发现可能解释HIA-DQ和HLA-DR位点的联合出现较单独出现表现对1型糖尿病有更高的危险性。 HLA与1型糖尿病亚型:按照HLA表现型对1型糖尿病亚型化,对临床和病因的区别是有意义的。一般认为若HLA表现为HLA-DR3/DR3将导致原发性自身免疫疾病,而HLA-DR4/DR4代表原发性环境因素为主要诱因,结果为继发性自身免疫反应。伴有HLA-DR3的1型糖尿病常合并存在其他自身免疫性疾病(如肾上腺皮质功能不足、桥本甲状腺炎等),并以女性多见,起病年龄较大。而伴有HLA-DR4的1型糖尿病患者与其他免疫内分泌疾病几乎无关,以男性多见,起病年龄较轻。有报告745例1~19岁起病的1型糖尿病患者,根据HLA分型显示:HLA-DR3患者较HLA-DR4患者起病时病情较轻,酮尿轻,随后部分缓解的倾向大。 2.环境因素 1型糖尿病发生常与某些感染有关或感染后随之发生。常见的感染原有腮腺炎病毒、风疹病毒、巨细胞病毒、麻疹病毒、流感病毒、脑炎病毒、脊髓灰质炎病毒、柯萨奇病毒及Epstein-Barr病毒等,但病毒感染后,糖尿病发生的易感性或抵抗性可能由先天决定。若两个人(如同胞兄弟或姐妹)暴露于同样的病毒感染,可能表现为病毒抗体的相同升高,然而糖尿病可能仅在一个人身上发生,这可能是由于内在的遗传易感因素的差异。易感性可能意味B细胞对某一病毒特定剂量的敏感性;或对某一表达在B细胞病毒抗原或轻微B细胞损害过程中释放的自身抗原发生自身免疫反应的倾向性。 最近有一些研究报告出生后3个月内用牛奶或牛奶制品配方喂养的儿童发生1型糖尿病的危险性较高,引起不少关注。研究认为牛奶中某些蛋白质成分可能是导致糖尿病的因素之一,如牛血清白蛋白,已在大多数1型糖尿病患者体内检测到针对牛血清蛋白的抗体,该抗体能与胰岛B细胞溶解物中的分子量69000蛋白质发生沉淀。抗体的产生被认为是由于婴幼儿肠道通透性允许蛋白质进入循环,循环中的牛血清白蛋白引起淋巴细胞致敏,发生与胰岛B细胞69000蛋白质交叉的体液和细胞免疫反应,最终导致B细胞破坏。另2种蛋白为β乳球蛋白和酪蛋白,亦被认为是1型糖尿病的独立危险因素。也有推测应用较高热量配方的牛奶喂养婴儿可在幼年期引起胰岛素分泌升高和胰岛B细胞抗原递呈作用增强。但也有认为牛奶与1型糖尿病的关系不明确,有关牛奶蛋白作为1型糖尿病的始发因素仍有较大的争论,有待更进一步研究。 3.遗传-环境因素相互作用 遗传和环境因素对某个体1型糖尿病发病的影响程度不一。有关环境因素如何启动胰岛B细胞的自身免疫反应过程仍不完全清楚,一般情况下,人类l型糖尿病需要易感性的遗传背景,即一些环境物质诱发具有遗传易感性个体B细胞发生自身免疫。假说:一旦环境因素对B细胞的损害超过个体遗传决定的B细胞损害的耐受程度,此时便发生1型糖尿病。具体见图1。
环境因素通过释放细胞因子如白介素-1(IL-1)或肿瘤坏死因子-α(TNF-α)等特异或非特异性损害B细胞。遗传因素起到允许作用和决定B细胞最初损害自身免疫启动的易感性。罕见的情况是:特异性B细胞毒物质跨过自身免疫导致B细胞大量受损。比较常见的情况是:反复的B细胞损伤在遗传易感的个体中诱发继发性抗B细胞自身免疫;如此自身免疫亦可能在无环境因素的参与下而自发发生。B细胞死亡的最终共同途径可能来自产生的过多氧自由基或NO对B细胞的破坏。 2型糖尿病的病因不是十分明确,现一般认为是具有强烈的遗传或为多基因遗传异质性疾病,环境因素有肥胖、活动量不足和老龄化等。其发病主要是由于胰岛素抵抗为主伴胰岛素分泌不足,胰岛素抵抗一般先于胰岛素分泌障碍;或胰岛素分泌不足为主伴或不伴有胰岛素抵抗。虽2型糖尿病具有遗传异质性,但大多数伴2型糖尿病和空腹高血糖的患者特征性表现为胰岛素抵抗、胰岛素分泌障碍和肝脏葡萄糖产生增加。